Équation de Mayo-Lewis
L'équation de Mayo-Lewis concerne l'obtention de copolymères diblocs par polyaddition. Elle sert à relier la composition instantanée du copolymère à la composition du mélange de monomères.
L'équation de Mayo-Lewis concerne l'obtention de copolymères diblocs par polyaddition. Elle sert à relier la composition instantanée du copolymère (pourcentage d'unités A et B) à la composition du mélange de monomères (pourcentage de monomères A et B). Elle donne aussi une idée de la structure du copolymère : statistique, à bloc, alterné…
L'équation est la suivante :
![\frac {\mathrm{d}[A]} {\mathrm{d}[B]} = \frac {[A]}{[B]} \frac {r_A[A] + [B]} {r_B[B] + [A]}](illustrations/20f4e2d8f044bfe0ec0c20f999c0d65a.png)
Les concentrations en monomères sont données entre crochets, rA et rB sont les rapports de réactivité.
Contexte et démonstration
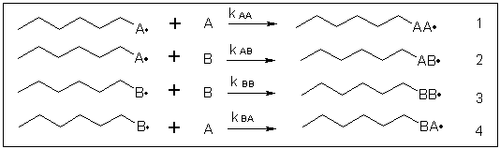
On synthétise un copolymère à partir des monomères A et B, en chaîne. À chaque addition d'un nouveau motif, on a quatre cas envisageables :
On cherche à savoir quelle sera la proportion des unités monomères issues de A et B dans le copolymère constitué. On peut écrire la vitesse de disparition des deux monomères :
![- \frac { \mathrm{d}[A] } { \mathrm{d}t } = k_{AA} [Aˆ\bullet][A] + k_{BA} [Bˆ\bullet][A]](illustrations/9cb965353f44d882a46f498eece4f692.png)
![- \frac { \mathrm{d}[B] } { \mathrm{d}t } = k_{BB} [Bˆ\bullet][B] + k_{AB} [Aˆ\bullet][B]](illustrations/1971084cade4ba236f5639c2793bed11.png)
Dans l'hypothèse de l'ÆQS, ![k_{AB} [Aˆ\bullet][B] = k_{BA} [Bˆ\bullet][A]](illustrations/78523cd09d61bf21f92a61c06eb5c2c0.png) La concentration en centres actifs reste constante.
La concentration en centres actifs reste constante.
En faisant le rapport des deux vitesses de disparition en tenant en compte de cette cette égalité, on obtient : ![\frac {\mathrm{d}[A]} {\mathrm{d}[B]} = \frac {[A]}{[B]} \frac {\frac {k_{AA}}{{k_{AB}}}[A] + [B]} {\frac {k_{BB}}{{k_{BA}}}[B] + [A]}](illustrations/6162df80ecf2d6984059e14fb287e072.png)
On peut introduire les rapports de réactivité : 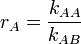 et
et 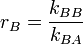 .
.
On aboutit à : ![\frac {\mathrm{d}[A]} {\mathrm{d}[B]} = \frac {[A]}{[B]} \frac {r_A[A] + [B]} {r_B[B] + [A]}](illustrations/20f4e2d8f044bfe0ec0c20f999c0d65a.png)
C'est l'équation de Mayo-Lewis[1].
Calcul de composition
On définit les fractions molaires :
- des unités monomères dans le copolymère constitué :
![F_A = 1 - F_B = \frac {\mathrm{d}[A]} {\mathrm{d}[A] + \mathrm{d}[B]}](illustrations/36f93e65d2426e16632dc4d0cd36ba46.png)
- des monomères dans le mélange de monomère :
![f_A = 1 - f_B = \frac {[A]} {[A] + [B]}](illustrations/dd31e2a145cec1a5899fd17825c5ea5a.png)
alors l'équation de Mayo-Lewis devient :
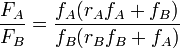
À partir de cette relation, si on connait les rapports de réactivité, on peut calculer la composition d'un mélange de monomères à maintenir constante pour aboutir a un copolymère de composition donnée.
Répartition des motifs
Selon les valeurs des rapports de réactivité rA et rB, on peut avoir une idée de la structure du copolymère. Ainsi, si kAA > kAB. dans ce cas, l'unité monomère A réagira préférentiellement sur elle-même plutôt que sur une unité B. Un certain nombre de cas limites existent.
- rA et rB << 1: les unités réagissent préférentiellement sur l'autre type et on obtient un copolymère alterné : (A − B − A − B − A − B − A − B − A − B − A − B) n
- rA et rB
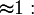 : les unités réagissent sur elles-même ou sur l'autre sorte indifféremment. Le copolymère est statistique[2] : (A − B − B − A − B − B − B − A − A − B − A − A) n
: les unités réagissent sur elles-même ou sur l'autre sorte indifféremment. Le copolymère est statistique[2] : (A − B − B − A − B − B − B − A − A − B − A − A) n - rA > 1 et rB < 1 : les unités de A réagissent entre elles et celles de b sur A aussi. Le copolymère enchaîne en particulier des unités A avec quelques accidents de B, jusqu'à ce que énormément d'unités A soient consommées : (A − A − B − A − A − A − A − B − A − A − A − A − B) .
- rA > 1 et rB > 1 : dans ce cas hypothétique la copolymérisation ne se ferait pas ou mal.
Calcul des rapports de réactivité
Si on pose : ![x = \frac {[A]}{[B]}](illustrations/7b054a2a036d97848253fdd57eb62026.png) et
et 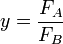 , l'équation de Mayo-Lewis devient :
, l'équation de Mayo-Lewis devient : 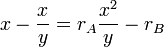
On peut préparer des copolymères de compositions différentes et tracer 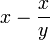 selon
selon 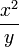 . La courbe obtenue est une droite dont la pente et l'ordonnée à l'origine permettent de remonter aux rapports de réactivité. D'autres méthodes existent.
. La courbe obtenue est une droite dont la pente et l'ordonnée à l'origine permettent de remonter aux rapports de réactivité. D'autres méthodes existent.
Références
Voir aussi
Recherche sur Google Images : |
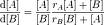
"en monomères sont données" L'image ci-contre est extraite du site fr.wikipedia.org Il est possible que cette image soit réduite par rapport à l'originale. Elle est peut-être protégée par des droits d'auteur. Voir l'image en taille réelle (196 × 47 - 2 ko - png)Refaire la recherche sur Google Images |
Recherche sur Amazone (livres) : |
Voir la liste des contributeurs.
La version présentée ici à été extraite depuis cette source le 13/12/2010.
Ce texte est disponible sous les termes de la licence de documentation libre GNU (GFDL).
La liste des définitions proposées en tête de page est une sélection parmi les résultats obtenus à l'aide de la commande "define:" de Google.
Cette page fait partie du projet Wikibis.


 Accueil
Accueil Recherche
Recherche Début page
Début page Contact
Contact Imprimer
Imprimer Accessibilité
Accessibilité